抗うつ作用に重要な脳の領域を発見―新しいうつ病治療法の開発に期待―
研究成果の概要
名古屋市立大学大学院医学研究科統合解剖学分野・内田周作准教授(研究当時、京都大学大学院医学研究科メディカルイノベーションセンター特定准教授)、京都大学大学院医学研究科創薬医学講座・大槻元特定教授、同研究科精神医学・村井俊哉教授、大石直也特定准教授、マウントサイナイ医科大学・九野(川竹)絢子大学院生(研究当時、京都大学医学部附属病院研修医)らの研究グループは、新しい抗うつ薬として期待されているケタミン誘導体による持続的な抗うつ作用には視床室傍核とよばれる脳の領域が重要であること、そして分子メカニズムを発見しました。既存の抗うつ薬は効果発現まで時間を要すること、治療効果が限定的であること、再燃しやすいことが問題となっています。本研究成果から、持続性を有する新しいタイプの抗うつ薬の開発につながることが期待できます。
本研究成果は、2024年2月20日(日本時間)に、米科学誌「Neuron」電子版に掲載されました。
本研究成果は、2024年2月20日(日本時間)に、米科学誌「Neuron」電子版に掲載されました。
研究成果のポイント
- 麻酔薬ケタミンは低用量で難治性うつ病患者に即効性・持続性の抗うつ効果があることが明らかになり、うつ病の新規治療薬候補として注目されている。しかし、ケタミン並びにその誘導体の抗うつ作用メカニズムは不明である。
- ケタミン誘導体の1つであるS-HNKに着目し、S-HNKによる持続的な抗うつ作用の脳内メカニズム解明を試みた。
- S-HNKによる持続的な抗うつ効果には、視床室傍核が関わること、並びにその分子機序を明らかにした。
- ケタミン誘導体の作用機序の解明により、持続性を有する新しいタイプの抗うつ薬の開発が期待できる。
背景
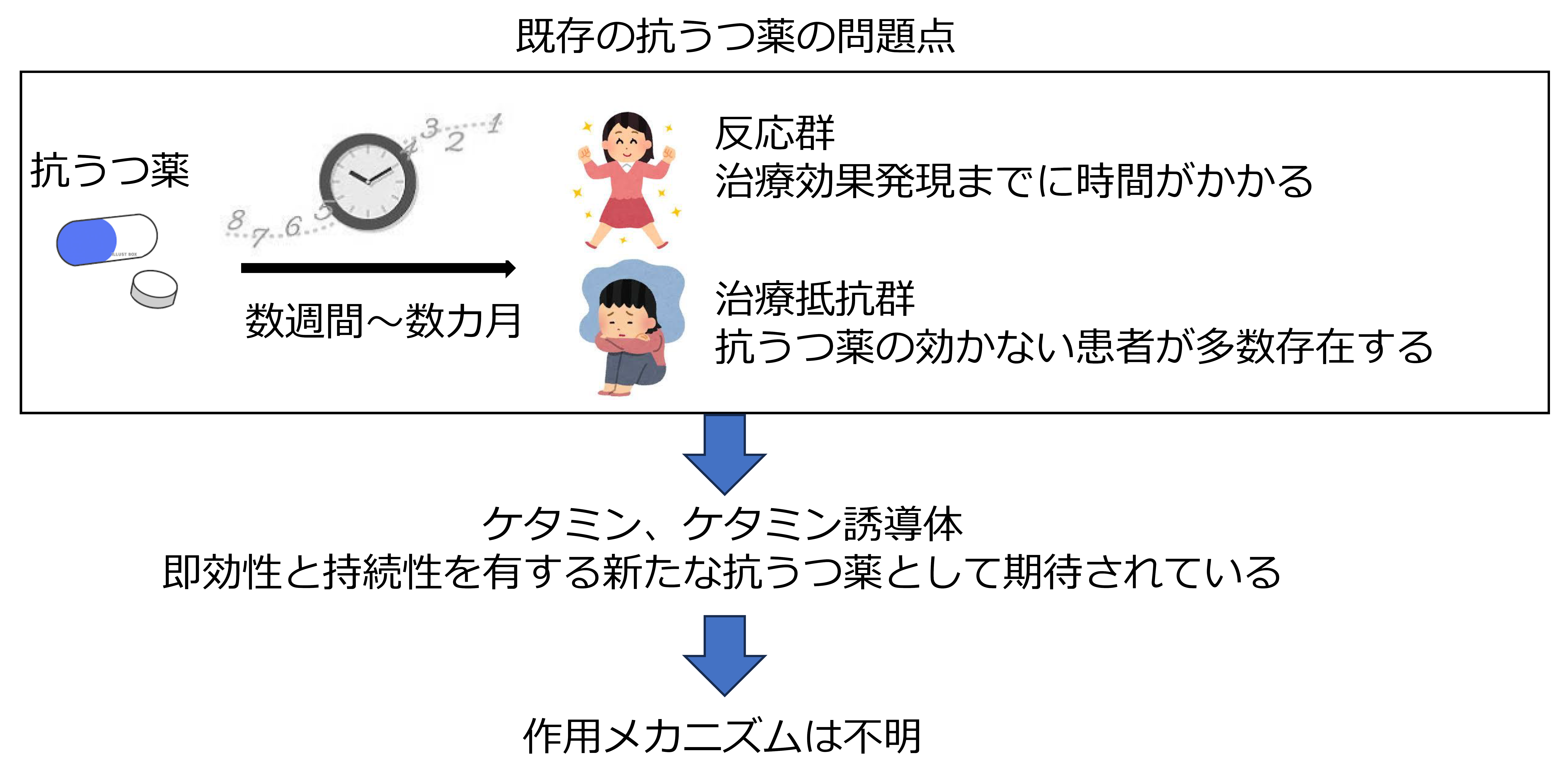
近年のストレス社会やコロナ禍・自然災害による生活様式の変化を背景に、うつ病(注1)などの精神疾患を発症する人が増加しています。うつ病に対する治療薬として抗うつ薬が使用されていますが、既存のモノアミン系抗うつ薬(注2)は治療効果発現までに数週間単位の時間を要すること、治療抵抗性を示す患者が多く存在すること、再発しやすいこと、等が問題となっています。そのため、即効性と持続性を有する新たな抗うつ薬の開発が望まれています。
そのような中、麻酔薬として使用されているケタミン(注3)が低用量で即効性と持続性の抗うつ作用を有する薬剤として注目されており、ケタミンの抗うつ効果はうつ病研究の歴史において過去60年間で最も大きな発見とまで言われています。ケタミンは2つの光学異性体を有し、最終的に(2S,6S)-hydroxynorketamine (S-HNK) と(2R,6R)-HNK (R-HNK)に代謝されます。ケタミンには依存性・幻覚・多動などの重篤な副作用がありますが、ケタミン誘導体にはそのような副作用は少ないことが知られており、より安全性の高い治療薬として期待されます。しかし、これらケタミン誘導体による抗うつ作用メカニズムは不明でした。
そこで研究グループは、ストレスを負荷したうつ病モデルマウスを用いて、副作用の少ないS-HNKによる持続的な抗うつ効果とそのメカニズム解明を試みました。
そのような中、麻酔薬として使用されているケタミン(注3)が低用量で即効性と持続性の抗うつ作用を有する薬剤として注目されており、ケタミンの抗うつ効果はうつ病研究の歴史において過去60年間で最も大きな発見とまで言われています。ケタミンは2つの光学異性体を有し、最終的に(2S,6S)-hydroxynorketamine (S-HNK) と(2R,6R)-HNK (R-HNK)に代謝されます。ケタミンには依存性・幻覚・多動などの重篤な副作用がありますが、ケタミン誘導体にはそのような副作用は少ないことが知られており、より安全性の高い治療薬として期待されます。しかし、これらケタミン誘導体による抗うつ作用メカニズムは不明でした。
そこで研究グループは、ストレスを負荷したうつ病モデルマウスを用いて、副作用の少ないS-HNKによる持続的な抗うつ効果とそのメカニズム解明を試みました。
研究の背景
研究の成果
ケタミン誘導体による抗うつ作用
マウスに繰り返しの心理社会ストレスを負荷し、うつ様行動の指標と考えられている社交性と無快感症(アンヘドニア)を評価する行動試験を行いました。その後、マウスのうつ状態と考えられる行動異常を示したマウスにS-HNKを投与し、一定時間後に再度行動評価を行いました。その結果、S-HNK投与マウスは30分後に抗うつ作用を認め、その効果は28日間持続していました。
S-HNK反応群に特徴的な脳部位の抽出と同定
S-HNKあるいはR-HNKを投与したマウスを用いてFos(注4)発現マッピングにより脳内神経活動を調べたところ、各薬剤に特徴的な脳部位を抽出することができました。特に、持続的な抗うつ作用を有するS-HNKに特徴的な脳部位として視床室傍核(注5)を見出しました。
そこで、視床室傍核の機能を人為的に抑制したマウスを作製したところ、S-HNKによる持続的な抗うつ作用は消失していました。逆に視床室傍核の機能を人為的に活性化したところ、S-HNK投与マウスに類似した行動変容(社交性の回復、アンヘドニアの消失=抗うつ効果)を示しました。これらの結果から、視床室傍核がS-HNKによる持続的な抗うつ作用に必須の脳領域であることが示されました。
S-HNKによる持続的な抗うつ作用の脳内分子メカニズム解析
S-HNKによる持続的な抗うつ作用に視床室傍核が必須であることが分かりました。そこで、持続的な抗うつ作用に関わる視床室傍核内における分子メカニズム同定を試みました。網羅的遺伝子発現解析と因果性検証の結果、S-HNKによる持続性抗うつ作用に関わる以下の分子パスウェイを新たに同定することに成功しました。
マウスに繰り返しの心理社会ストレスを負荷し、うつ様行動の指標と考えられている社交性と無快感症(アンヘドニア)を評価する行動試験を行いました。その後、マウスのうつ状態と考えられる行動異常を示したマウスにS-HNKを投与し、一定時間後に再度行動評価を行いました。その結果、S-HNK投与マウスは30分後に抗うつ作用を認め、その効果は28日間持続していました。
S-HNK反応群に特徴的な脳部位の抽出と同定
S-HNKあるいはR-HNKを投与したマウスを用いてFos(注4)発現マッピングにより脳内神経活動を調べたところ、各薬剤に特徴的な脳部位を抽出することができました。特に、持続的な抗うつ作用を有するS-HNKに特徴的な脳部位として視床室傍核(注5)を見出しました。
そこで、視床室傍核の機能を人為的に抑制したマウスを作製したところ、S-HNKによる持続的な抗うつ作用は消失していました。逆に視床室傍核の機能を人為的に活性化したところ、S-HNK投与マウスに類似した行動変容(社交性の回復、アンヘドニアの消失=抗うつ効果)を示しました。これらの結果から、視床室傍核がS-HNKによる持続的な抗うつ作用に必須の脳領域であることが示されました。
S-HNKによる持続的な抗うつ作用の脳内分子メカニズム解析
S-HNKによる持続的な抗うつ作用に視床室傍核が必須であることが分かりました。そこで、持続的な抗うつ作用に関わる視床室傍核内における分子メカニズム同定を試みました。網羅的遺伝子発現解析と因果性検証の結果、S-HNKによる持続性抗うつ作用に関わる以下の分子パスウェイを新たに同定することに成功しました。
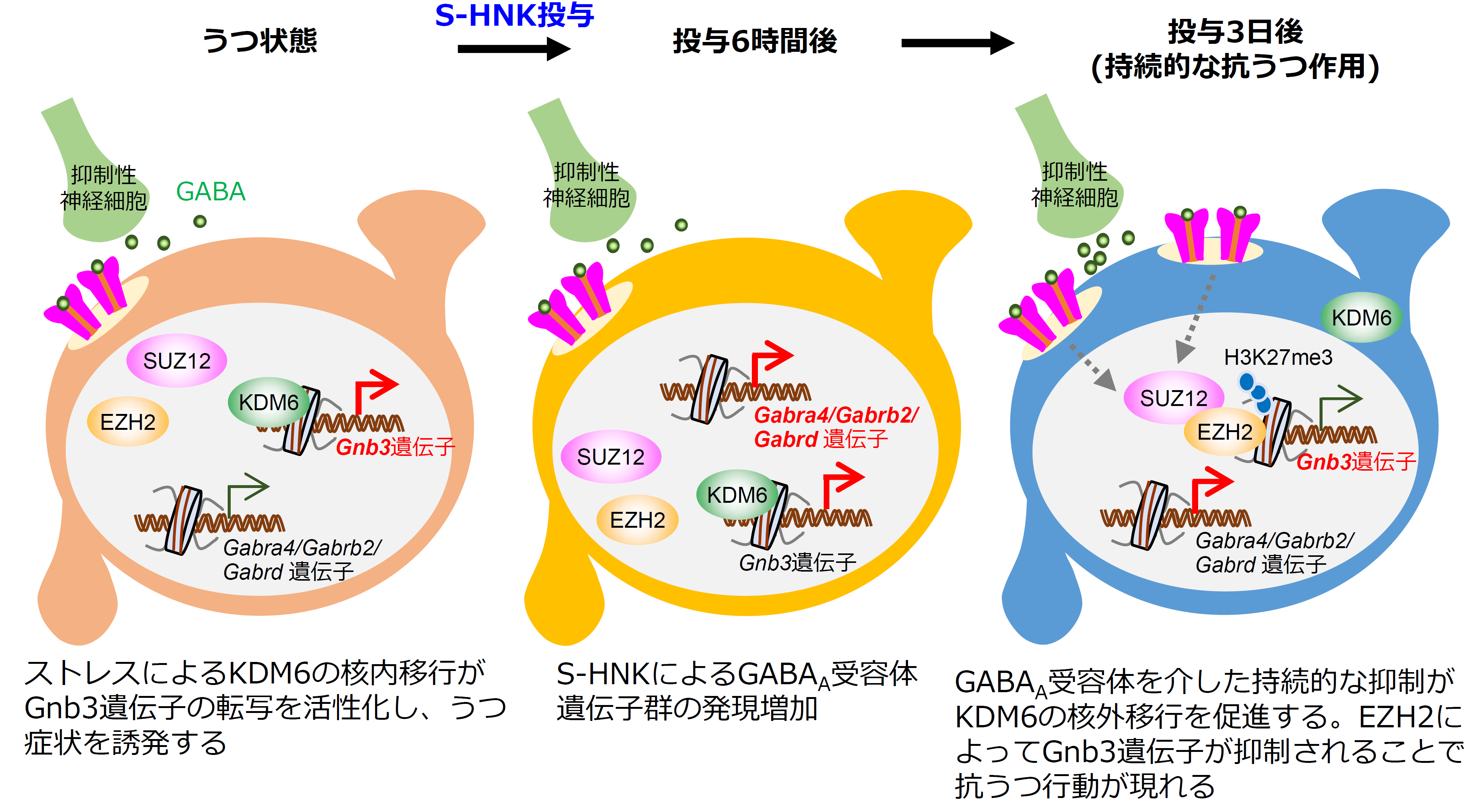
- ストレス負荷により視床室傍核グルタミン酸作動性ニューロン内でGnb3遺伝子の転写が亢進してうつ状態を誘発
- S-HNKによるGABAA受容体の発現増加(投与後6時間)
- 視床室傍核グルタミン酸作動性ニューロンの持続的な抑制(投与後3日)
- 視床室傍核グルタミン酸作動性ニューロンにおけるエピジェネティクス制御分子の機能変容と標的遺伝子の発現調節(投与後3日):S-HNKによるGABAA受容体の機能亢進によってヒストン脱メチル化酵素KDM6の核外移行が促進され、ヒストンメチル基転移酵素EZH2が優位に働く。その結果、標的遺伝子であるGnb3の発現が低下し、抗うつ行動を誘発する。
研究結果のまとめ (発表論文の図を一部改変)
研究の意義と今後の展開や社会的意義など
今回の研究から、ケタミン誘導体のS-HNKが持続的な抗うつ作用を発揮すること、さらにそのメカニズムとして視床室傍核が関わること、GABAA受容体の抑制性シグナルによる遺伝子発現制御機構が重要な役割を果たしていることが明らかとなりました。今回の成果はストレスが引き金となって発症するうつ病や不安症に対する治療法の開発、うつ病の再発予防法の開発につながる可能性があります。S-HNK自体が薬剤として使用できる可能性に加え、今回明らかにしたS-HNKの分子神経メカニズムを基盤とした治療薬の開発が期待されます。
【用語解説】
注1)うつ病
米国の操作的診断基準であるDSM-5では、うつ病は「抑うつ気分」と「興味・喜びの喪失」の2つの主要症状が基本となる。「抑うつ気分」とは、気分の落ち込みや空虚感・悲しさなどである。「興味・喜びの喪失」とは、以前楽しめていたこと(趣味など)にも楽しみを見いだせない状態である。これら主要症状に加えて、「自分には何の価値もないと感じる無価値感」や「自殺念慮・希死念慮」などの症状がある。うつ病は未だ効果的な治療法のないアンメットメディカルニーズの高い疾患である。
注2)モノアミン系抗うつ薬
国内で処方されている抗うつ薬は、細胞外のモノアミン(セロトニンやノルアドレナリン)量を増加させる作用を有する薬剤である。これらの抗うつ薬は効果発現までに数週間以上の期間を要すること、3分の1以上のうつ病患者では治療効果が見られないこと、が問題となっている。
注3)ケタミン
1962年に合成された麻酔薬。既存の抗うつ薬に効果を示さない治療抵抗性うつ病患者に対して低用量のケタミンを静脈内に投与すると、数時間以内という短時間で抗うつ作用が現れ、その抗うつ作用は1週間程度持続すると報告されている。希死念慮・自殺願望の低下という既存の抗うつ薬にはない効果も有すると報告されている。
注4)Fos
細胞への刺激に応答して速やかに発現が誘導される最初期遺伝子の1つ。そのため、c-Fos遺伝子の発現(mRNAあるいはタンパク質レベル)は、脳内の機能的活性を評価するマーカー (神経活動マーカー) として広く使用されている。
注5)視床室傍核
脳の皮質下にある視床を構成する視床亜核群の一つで、恐怖記憶、不安、報酬、睡眠、摂食などに関わるとされる。
【研究助成】
本研究は、日本学術振興会科学研究費補助金(JP22H03532, JP21H00198, JP21K19707, JP19H04905, JP21K15711, JP21K07593, JP21H02849, 21H04795, JP21H05173)、AMED (JP23ak0101197, JP23ama121041j0002, JP22dm0307102)、日本科学技術振興機構JST-CREST (JPMJCR14L2)、塩野義製薬(SKプロジェクト)の支援を受けて行われました。
【論文タイトル】
Sustained antidepressant effects of ketamine metabolite involve GABAergic inhibition-mediated molecular dynamics in aPVT glutamatergic neurons
(ケタミン誘導体による持続的抗うつ作用はaPVTグルタミン酸作動性ニューロンにおけるGABA抑制調節的な分子ダイナミクスが関与している)
【著者】
九野(川竹)絢子1,2、李海燕1、稲葉啓通1、彦坂桃花1、石森絵里奈1、植木孝俊3、Yury Garkun2、森下博文2、成宮周1、大石直也1、大槻元1,*、村井俊哉1、内田 周作1,3,* (*責任著者)
所属:1京都大学大学院医学研究科, 2マウントサイナイ医科大学, 3名古屋市立大学大学院医学研究科
【掲載学術誌】
学術誌名 Neuron (ニューロン)
D O I: https://doi.org/10.1016/j.neuron.2024.01.023
【用語解説】
注1)うつ病
米国の操作的診断基準であるDSM-5では、うつ病は「抑うつ気分」と「興味・喜びの喪失」の2つの主要症状が基本となる。「抑うつ気分」とは、気分の落ち込みや空虚感・悲しさなどである。「興味・喜びの喪失」とは、以前楽しめていたこと(趣味など)にも楽しみを見いだせない状態である。これら主要症状に加えて、「自分には何の価値もないと感じる無価値感」や「自殺念慮・希死念慮」などの症状がある。うつ病は未だ効果的な治療法のないアンメットメディカルニーズの高い疾患である。
注2)モノアミン系抗うつ薬
国内で処方されている抗うつ薬は、細胞外のモノアミン(セロトニンやノルアドレナリン)量を増加させる作用を有する薬剤である。これらの抗うつ薬は効果発現までに数週間以上の期間を要すること、3分の1以上のうつ病患者では治療効果が見られないこと、が問題となっている。
注3)ケタミン
1962年に合成された麻酔薬。既存の抗うつ薬に効果を示さない治療抵抗性うつ病患者に対して低用量のケタミンを静脈内に投与すると、数時間以内という短時間で抗うつ作用が現れ、その抗うつ作用は1週間程度持続すると報告されている。希死念慮・自殺願望の低下という既存の抗うつ薬にはない効果も有すると報告されている。
注4)Fos
細胞への刺激に応答して速やかに発現が誘導される最初期遺伝子の1つ。そのため、c-Fos遺伝子の発現(mRNAあるいはタンパク質レベル)は、脳内の機能的活性を評価するマーカー (神経活動マーカー) として広く使用されている。
注5)視床室傍核
脳の皮質下にある視床を構成する視床亜核群の一つで、恐怖記憶、不安、報酬、睡眠、摂食などに関わるとされる。
【研究助成】
本研究は、日本学術振興会科学研究費補助金(JP22H03532, JP21H00198, JP21K19707, JP19H04905, JP21K15711, JP21K07593, JP21H02849, 21H04795, JP21H05173)、AMED (JP23ak0101197, JP23ama121041j0002, JP22dm0307102)、日本科学技術振興機構JST-CREST (JPMJCR14L2)、塩野義製薬(SKプロジェクト)の支援を受けて行われました。
【論文タイトル】
Sustained antidepressant effects of ketamine metabolite involve GABAergic inhibition-mediated molecular dynamics in aPVT glutamatergic neurons
(ケタミン誘導体による持続的抗うつ作用はaPVTグルタミン酸作動性ニューロンにおけるGABA抑制調節的な分子ダイナミクスが関与している)
【著者】
九野(川竹)絢子1,2、李海燕1、稲葉啓通1、彦坂桃花1、石森絵里奈1、植木孝俊3、Yury Garkun2、森下博文2、成宮周1、大石直也1、大槻元1,*、村井俊哉1、内田 周作1,3,* (*責任著者)
所属:1京都大学大学院医学研究科, 2マウントサイナイ医科大学, 3名古屋市立大学大学院医学研究科
【掲載学術誌】
学術誌名 Neuron (ニューロン)
D O I: https://doi.org/10.1016/j.neuron.2024.01.023

